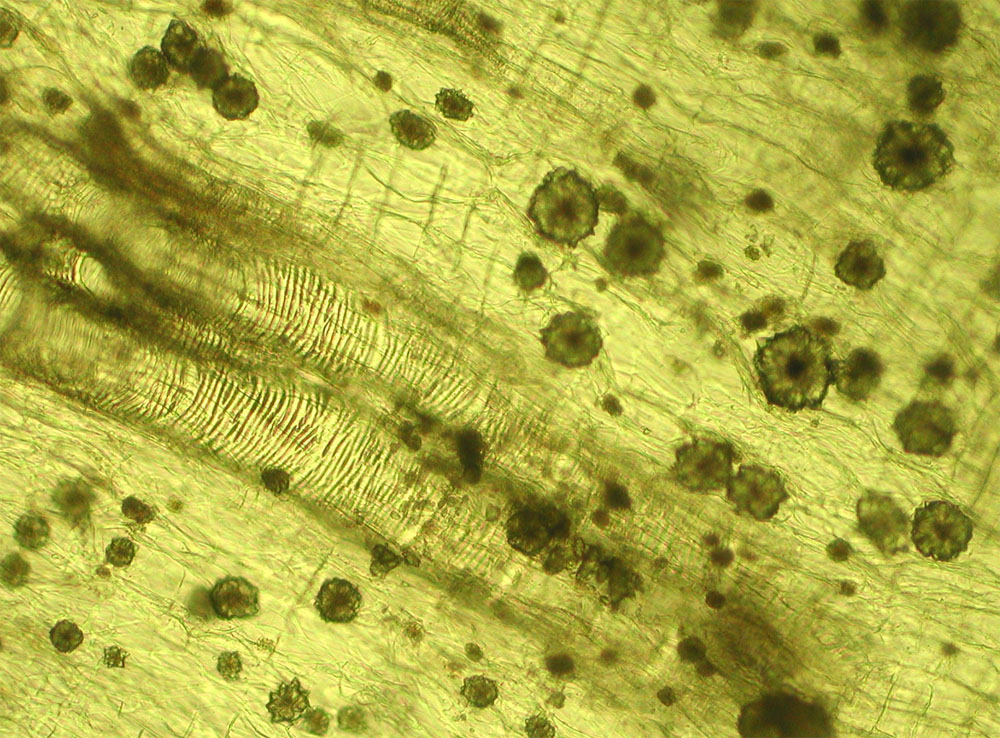
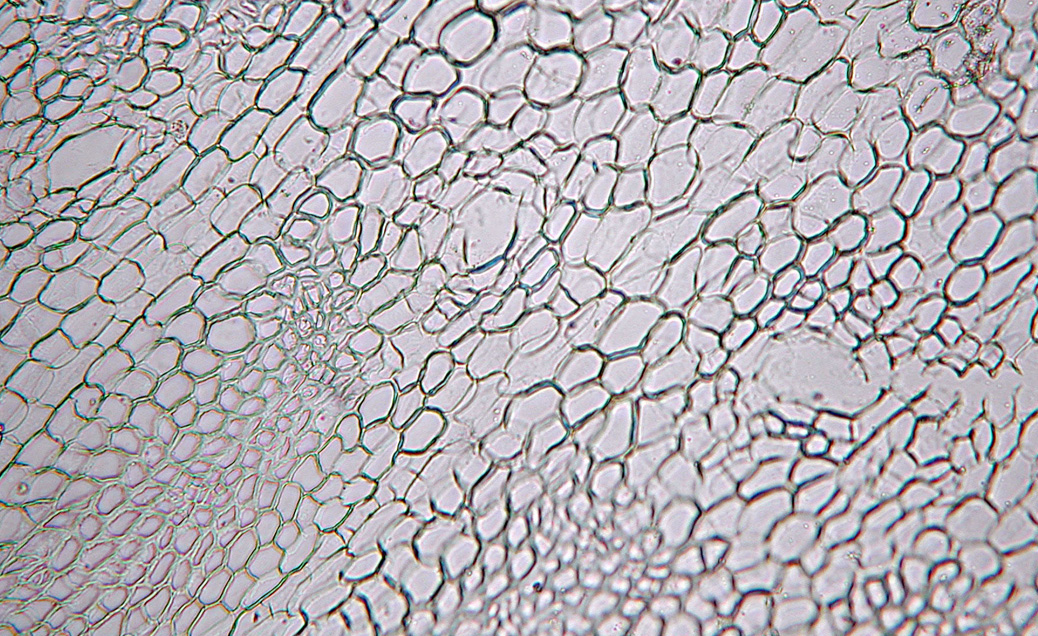
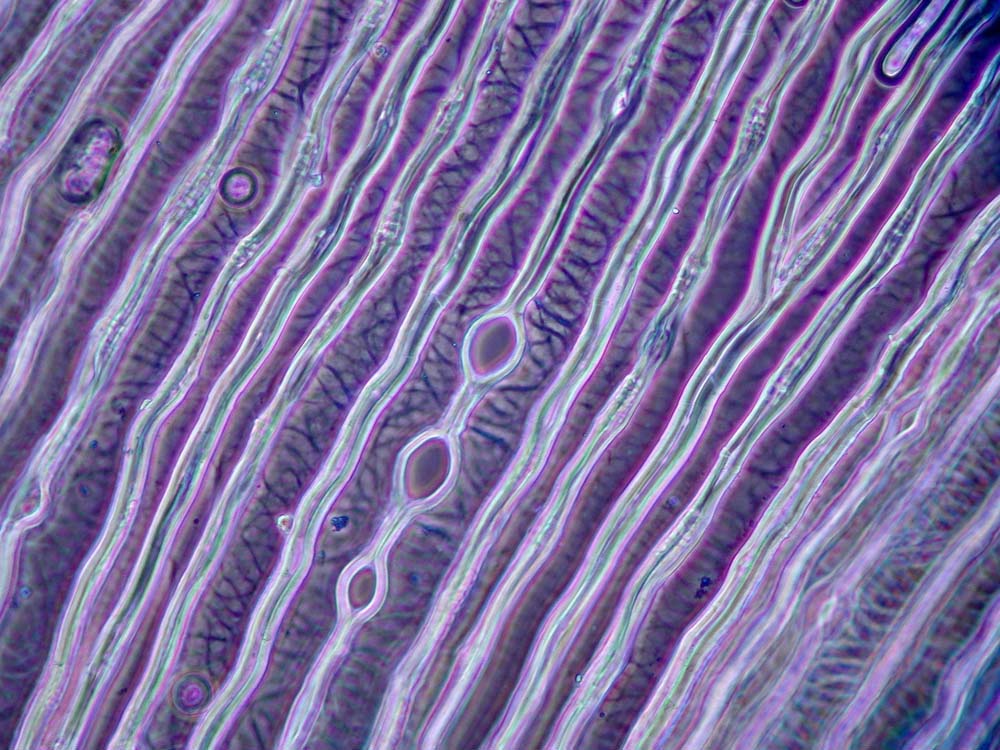
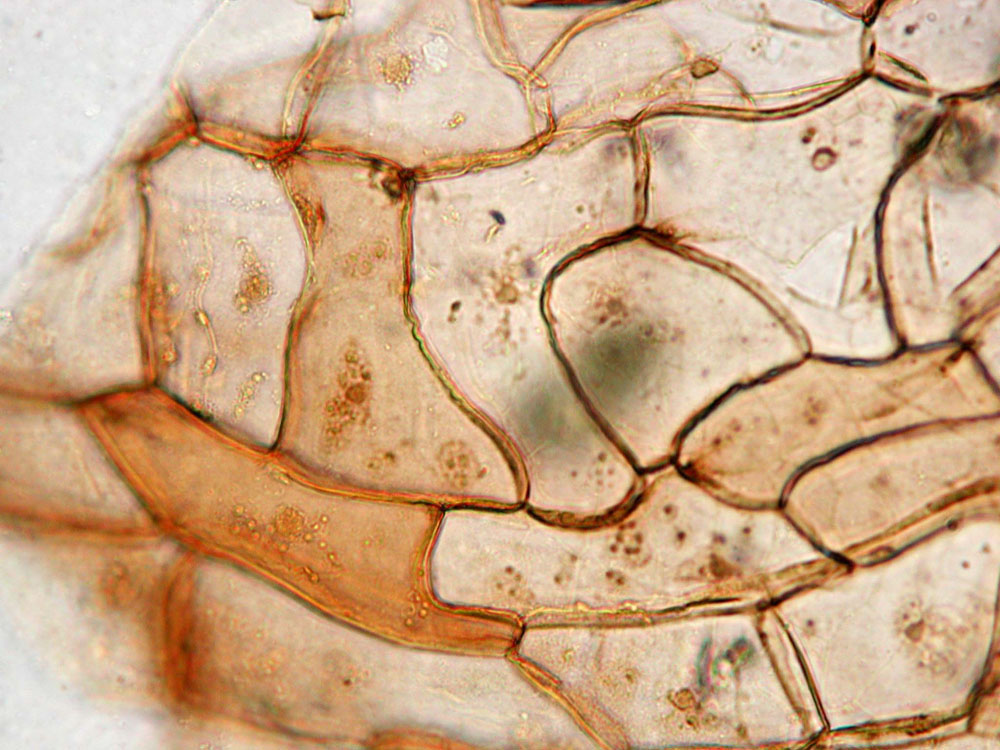
Asari Radix et Rhizoma, Xi xin
Verbot von Asarum, eine fragwürdige Sicherheitsphilosophie
Dt Zschr Akupunktur 54(2), 2011:47-50
Banning of Asarum – A Case of Questionable Safety Measures
Nachdem in den 90’er Jahren bekannt wurde, dass Aristolochiasäure(AA)-I und –II eine schwere Nephropathie und urotheliale Karzinome hervorgerufen können, fielen auch Aristolochiasäuregehalte in Asarumarten auf. Die in der Literatur veröffentlichten AA-I und AA-II-Gehalte sind jedoch meist gering und liegen teilweise unter der Nachweisgrenze. Im Jahre 2010 wurde in der Schweiz und in Deutschland die Verwendung von Pflanzen der Gattung Asarum in Arzneimitteln verboten. Verglichen mit dem, was bei konventionellen Arzneimitteln oder bei Risiken des täglichen Lebens toleriert wird, ist die die Risikotoleranz hier extrem niedrig angesetzt. Das Totalverbot von Asarum erscheint unangemessen.
Wegen der Aristolochiasäuregehalte wurde im Jahre 2010 in der Schweiz und in Deutschland die Verwendung von Pflanzen der Gattung Asarum in Arzneimitteln verboten. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) geht bei diesem Verbot davon aus, dass bei 2jähriger Anwendung ein 50prozentiges Tumorrisiko für die Lebenszeit bei höchstens einer von 1.000.000 Personen tolerabel sei. Dieses Sicherheitsrisiko ist verglichen mit dem, was bei konventionellen Arzneimitteln oder bei Risiken des täglichen Lebens toleriert wird, extrem niedrig angesetzt. Bei einer realistischeren Risikokalkulation, die zahlenmäßig im Bereich des Todesfallrisikos liegt, das für die Gesamtbevölkerung durch den Betrieb von kerntechnischen Anlagen in Deutschland pro Expositionsjahr toleriert wird, könnte das Gesundheitsrisiko durch Begrenzung der Anwendungsdauer und Verwendung von Xi xin-Drogen mit gesicherter Qualität ausreichend minimiert werden. Das Totalverbot von Asarum erscheint unangemessen.
Schlüsselwörter: Chinesische Arzneitherapie, Asarum, Xi xin, Aristolochiasäure, Nephropathie, Tumorrisiko, unerwünschte Arzneimittelreaktion
Abstract
Xi xin – radix et rhizoma asari – is a classical drug in Chinese medicine which is vitally important to various of applications that make it difficult to replace. After it became public in the 1990s that aristolochic acid (AA)-I and –II can cause nephropathia and urothelic carcinoma, aristolochic acid content of asarum species received quite some attention. The AA-I as well as AA-II contents documented in medical literature are actually low, in some cases even undetectable. Asarum crispulatum however, which is not officinal, is characterised by an extremely high AA content. Due to this, in 2010 the use of asarum species was banned in Germany and Switzerland. The Federal Institute for Drugs and Medicinal Devices (BfArM) concedes that during a 2-year use, a 50 % life time tumor risk is only tolerable in 1 out of 1,000,000 persons. Compared to conventional drugs as well as to every day life risks, the safety threshold in this case seems unusually low. By applying more realistic calculations similar to, for instance, the casualty risk for the entire population posed by the use of nuclear energy in Germany per annum, health risks could be controlled by limiting the duration of use, as well as enforcing strict quality control measures on xi xin drugs. A total ban of asarum species, however, seems inappropriate.
Key words: Chinese Herbal Medicine, Asarum, Xi xin, aristolochic acid, nephropathia, tumor risk, adverse drug event
Xi xin – Radix et Rhizoma Asari – ist eine klassische Droge der chinesischen Medizin, die schon in der ersten überlieferten Materia Medica, dem shen nong ben cao jing aus der späten Han-Zeit enthalten war. In der Chinesischen Medizin hat xi xin die Qualitäten scharf und warm, öffnet die Oberfläche, zerstreut Kälte, leitet Wind, Kälte, Feuchtigkeit und Schleim aus und beseitigt Schmerz. Es wird besonders bei Erkältungen, Husten mit dünnflüssigem Sputum sowie Kopf-, Zahn- und Gelenkschmerzen verwendet. Es ist für verschiedene Anwendungen eine essentielle Droge, die durch andere Mittel schwer zu ersetzen ist.
Traditionell ist die Droge vorsichtig zu dosieren, die offizielle Tagesdosis liegt bei 1 bis 3g Rohdroge [1]. Überdosierung kann zu Nebenwirkungen bis hin zu letalem Ausgang führen [2, 3]. Die toxischen Reaktionen werden auf den Inhaltsstoff Safrol zurückgeführt [3]. Safrol gilt auch als schwach hepatocancerogen und gentoxisch. Durch Dekoktieren wird der Gehalt erheblich reduziert und dann als tolerabel angesehen. [4].
Eine ganz andere Problematik tauchte auf, als in den 90’er Jahren Aristolochiasäuren in chinesischen Aristolochia-Drogen als Ursache für eine Reihe schwerer Nephropathien identifiziert wurden, die in einer Belgischen Schlankheitsklinik aufgetreten waren. In der Folge wurden weltweit weitere Fälle aufgedeckt [5], viele davon entwickelten urotheliale Karzinome [6]. Aristolochiasäuren waren schon vorher als stark krebserregend bekannt und hatten 1981 in Deutschland zum Verbot Aristolochiasäure-haltiger Arzneimittel geführt [5]. Im Zuge der in verschiedenen Ländern eingeleiteten Vorsichtsmaßnahmen und Verbote fiel auch ein Aristolochiasäure-Gehalt bei Asarum-Arten auf, der jedoch, wenn er überhaupt nachweisbar war, deutlich unter den bei den Aristolochia-Drogen gemessenen Werten lag.
Um das Risiko zu minimieren, wurde in der Chinesischen Pharmakopöe von 2005 der offiziell verwendete Pflanzenteil, der vorübergehend wegen Beschaffungsproblemen auf Herba, also den oberirdischen Teil umgestellt worden war, auf Radix et Rhizoma geändert, weil diese Teile einen geringeren Aristolochiasäuregehalt aufweisen. In Hongkong wurde bereits 2004 der Vertrieb von Herba oder Planta tota von Asarum verboten und nur noch Radix zugelassen [7].
Aristolochiasäuregehalte in Asarum
Aus der Literatur gehen die in Tab. 1 wiedergegebenen Werte für Aristolochiasäuregehalte von in der Chinesischen Medizin verwendeten Asarumarten hervor [8-12]. Legt man die offizinellen Pflanzenspezies für xi xin und die offizinellen Pflanzenteile (Radix et Rhizoma bzw. Radix) zugrunde (grün unterlegt), so liegen die Werte für Aristolochiasäure-I (AA-I) fast alle unter 1 μg/g, nur ein Wert fällt mit 2,16 μg/g höher aus. Der Gehalt an Aristolochiasäure-II (AA-II) ist im Allgemeinen deutlich niedriger und nur in einem Teil der Arbeiten untersucht worden.
Die Arbeit von Zhao und Mitarbeitern [12] verglich bei mehreren Proben den AA-I-Wert für einen wässrigen Extrakt mit dem für einen methanolischen Extrakt. Bei methanolischer Extraktion findet man im Extrakt einen Großteil der pflanzeneigenen Aristolochiasäure wieder, während der wässrige Extrakt je nach Extraktionsbedingungen mehr oder weniger einem Dekokt entspricht. In diesem Fall wurden die Drogen 20 Minuten in Wasser eingeweicht und dann 40 Minuten lang gekocht. Man erkennt aus den Messwerten (s. Tab. 1), dass durch die wässrige Extraktion der Aristolochiasäuregehalt deutlich abgereichert wird, und zwar bei Radix um einen Faktor zwischen 4,7 bis 18,6. Da durch wässrige Extraktion auch Granulate hergestellt werden, ist ein analoger Sicherheitsabstand auch auf diese übertragbar. Xi xin sollte nicht in Form der pulverisierten Rohdroge eingenommen werden, da in diesem Fall der volle Aristolochiasäuregehalt zur Geltung kommt.
Andere Pflanzenteile, nämlich die oberirdischen Teile (Herba) bzw. die ganze Pflanze (Planta tota) enthalten deutlich höhere Aristolochiasäuregehalte, das Maximum der veröffentlichten Werte liegt bei bedenklichen 142 μg/g. Dramatisch wird es bei einer nicht-offizinellen Spezies, nämlich Asarum crispulatum, das in Sichuan als lokale Variante für xi xin verwendet wird, mit einem Wert von 3.376,9 μg/g [9]. Dieser Wert entspricht einem mittleren Bereich für Gehalte, wie sie in den folgenschweren Aristolochia-Drogen bestimmt wurden [8]. Hieraus ist ersichtlich, wie wichtig der Einsatz offizineller Drogen mit valider Identitätsbestimmung ist.
Verbot durch das BfArM
In Deutschland wurde – ähnlich wie bereits vorher in der Schweiz – mit Bescheid des BfArM vom 22.07.2010 die Verwendung von Pflanzen der Gattung Asarum in Arzneimitteln verboten [13]. Anlass war der Nachweis von AA-I in homöopathischen Urtinkturen von Asarum europaeum mit Werten von 5,1 und 2,7 μg/g. Im Bescheid wird auch auf Literaturangaben mit höheren Aristolochiasäuregehalten hingewiesen, darunter auch auf den oben genannten hohen Wert in Asarum crispulatum.
Bei der Abschätzung des Risikos geht das BfArM von einem tolerablen „cancer life time risk“ von 1:1.000.000 aus. Danach ergibt sich unter Zugrundelegung einer linearen Dosis-Wirkungs-Beziehung bei zweijähriger Aufnahme eine „virtually safe dose“ von 0,36 ng Aristolochiasäure pro Tag. Für Homöopathika wird der oben genannte höchste je für eine Asarum-Art veröffentlichte Aristolochiasäuregehalt von 3.377 μg/g zugrunde gelegt, dabei werde die tolerable Dosis erst ab einer Potenzstufe von D9 unterschritten, mit entsprechendem Sicherheitsabstand werden erst Potenzstufen ab D11 für unbedenklich erklärt. Geht man von den niedrigsten veröffentlichten Aristolochiasäuregehalten im Dekokt für offizinelle Drogen aus, nämlich 0,04 μg/g, so wird die „virtually safe dose“ bei Aufnahme von 1g xi xin gerade überschritten. Aber: Sind die Annahmen für die Berechnung realistisch?
Realitätsferne Sicherheitsvorgaben
Um es noch einmal klar zu formulieren: Das BfArM hält es für gerade noch tolerabel, dass durch Aufnahme von Aristolochiasäure in Phytotherapeutika in einem von 1 Million Fällen über die Lebenszeit gerechnet mit 50prozentiger Wahrscheinlichkeit ein Tumor auftritt.Dieser Sicherheitsfaktor liegt jedoch weit jenseits tolerierter Risiken bei konventionellen Arzneimitteln.
Nach der WHI-Studie erkrankten durch Hormonersatztherapie pro Jahr(!) und pro 1 Million gesunder Frauen 700 zusätzlich an koronarer Herzkrankheit, 800 zusätzlich an Schlaganfällen, 1.800 an venösen Thrombosen und 800 an invasivem Brustkrebs. Die dem gegenüberstehenden 500 Hüftfrakturen und 600 kolorektalen Karzinome weniger wiegen die Negativbilanz nicht auf [14]. Die Hormonersatztherapie ist immer noch zugelassen, wobei deren Sinnhaftigkeit hier nicht diskutiert werden soll. Das wegen eines erhöhten Herzinsuffizienz- und Frakturrisikos umstrittene Antidiabetikum Pioglitazon verursachte nach Auswertung zweier 3-Jahres-Studien bei den Studienteilnehmern 0,3 % (Absolutwert) mehr Blasenkrebs als unter Placebo oder Glibenclamid, das entspricht einer zusätzlichen Karzinominzidenz von 3.000 auf 1 Million innerhalb dieses 3-Jahres-Zeitraums [15].
Erst recht eklatant wird das Sicherheitsgefälle, wenn man allgemeine Risiken des täglichen Lebens heranzieht. So verursacht Tabakrauchen zum Zeitpunkt der Ersterhebung nach einer Untersuchung aus Großbritannien innerhalb von 20 Jahren, wenn man die Daten auf 1.000.000 Erwachsene hochrechnet, 99.485 Todesfälle (errechnet nach [16]). Dabei sind Tabakprodukte ohne Einschränkungen für jedermann im Erwachsenenalter erhältlich.
Sicherlich ist ein Risiko immer im Vergleich zum Nutzen zu bewerten. Die Arzneimittelbehörden verfahren dabei jedoch offensichtlich nach einer Alles-Oder-Nichts-Regel: Wenn die Wirksamkeit eines Arzneimittels – und sei sie auch von noch so geringem Ausmaß - mit Ia- oder zumindest Ib-Evidenz nachgewiesen ist, wird ein mitunter hohes Risiko akzeptiert, während bei ausschließlich erfahrungsbasiert belegtem Nutzen eine Quasi-Null-Risiko-Forderung gilt. Diese Vorgehensweise ist nicht akzeptabel und lebensfremd. Wie das Beispiel Tabakprodukte zeigt – und hier könnten weitere wie Alkohol, Luftverschmutzung usw. angeführt werden, gilt dieser Purismus in anderen Bereichen nicht, wobei das Ausmaß der diesbezüglich tolerierten Gesundheitsschäden nicht gutgeheißen werden soll. Es drängt sich der Eindruck auf, dass konventionelle und komplementäre Therapieverfahren mit zweierlei Maß gemessen werden, wofür wohl das vorherrschende Medizinparadigma verantwortlich zu machen ist.
Andere Möglichkeiten der Risikobegrenzung wären möglich
Eine realistischere und dennoch durchaus weitgehende Risikominimierung könnte z.B. folgendermaßen aussehen: Unter Heranziehung der Grundannahmen des BfArM (die hier nicht näher untersucht werden sollen) wird eine 50prozentige Wahrscheinlichkeit für das Auftreten eines Tumors in 1 auf 10.000 Personenfälle - über die Lebenszeit gerechnet - toleriert und die Anwendungsdauer bei einer Dosis von maximal 3g Droge pro Tag auf höchstens 6 Wochen begrenzt. Diese Limits könnten bei einem Aristolochiasäuregehalt von unter 0,1 μg/g im unter standardisierten Bedingungen hergestellten Dekokt (AA-I und AA–II zusammenaddiert) das Tumorrisiko auf das angegebene Maß begrenzen. Die Einhaltung dieses Maximalgehaltes wäre bei Verwendung offizineller Drogen mit niedrigem Aristolochiasäure-Gehalt möglich. Für Granulate könnte der Gehalt entsprechend dem Droge-Extrakt-Verhältnis bei reduzierter Maximaldosis höher liegen.
Die 50prozentige Wahrscheinlichkeit für das Auftreten eines Tumors in 1 auf 10.000 Personenfälle - über die Lebenszeit gerechnet - entspricht zahlenmäßig dem Krebstodrisiko, das bei einer in Deutschland durch den Betrieb von kerntechnischen Anlagen für die Gesamtbevölkerung zulässigen Strahlendosis von 1 mSv [17] für jedes Jahr der Exposition zu erwarten ist (errechnet unter Annahme einer linearen Dosis-Wirkungsbeziehung und Zugrundelegung von Risikodaten der Internationalen Strahlenschutzkommission ICRP, die das Risiko möglicherweise stark unterschätzen [18]).
Schlussfolgerung:
Qualitätsgesicherte xi xin-Drogen bzw. -Drogenextrakte und eine Begrenzung der Anwendungsdauer können das Krebsrisiko auf ein minimales und akzeptables Maß reduzieren. Dabei ist eine Prüfung auf Identität und auf den Aristolochiasäuregehalt mit ausreichend empfindlicher Methodik unumgänglich, zumal in China 30 verschiedene Asarum-Arten sowie 4 Unterarten vorkommen und Verfälschungen häufig sind [3]. Das Totalverbot von Asarum ist unangemessen und ein empfindlicher Verlust für die Therapieoptionen der Chinesischen Arzneitherapie.
Literatur:
- Pharmacopoeia of the People's Republic of China. Vol. I. Beijing: People's Medical Publishing House, 2005
- Drew AK, Whyte IM, Bensoussan A, et al. Chinese herbal medicine database: monograph on Herba Asari, "Xi Xin". Clin Toxicol 2002;40:169-172
- Bensky D, Clavey S and Stöger E. Chinese Herbal Medicine. Materia Medica. 3th ed. Seattle: Eastland Press, 2004
- Chen C, Spriano D, Lehmann T, et al. Reduction of safrole and methyleugenol in Asari radix et rhizoma by decoction. Forsch Komplementmed 2009;16:162-6
- Wiebrecht A. Über die Aristolochia-Nephropathie. Dt Zschr Akupunktur 2000;43:187-197
- Nortier JL, Martinez M-CM, Schmeiser HH, et al. Urothelial carcinoma associated with the use of a Chinese herb (Aristolochia fangchi). New Engl J Med 2000;342:1686-92
- Government of Hong Kong, Department of Health. Management of aristolochic acid (AA) containing herbs and products, 11 June 2004, http://www.cmchk.org.hk/pcm/news/AA_CMTraders_e.pdf
- Hashimoto K, Higuchi M, Makino B, et al. Quantitative analysis of aristolochic acids, toxic compounds, contained in some medical plants. J Ethnopharmacol 1999;64:185-9
- Jong TT, Lee MR, Hsiao SS, et al. Analysis of aristolochic acid in nine sources of Xixin, a traditional Chinese medicine, by liquid chromatography/atmospheric pressure chemical ionization/tandem mass spectrometry. J Pharm Biomed Anal 2003;33:831-7
- Schaneberg BT, Khan IA. Analysis of products suspected of containing Aristolochia or Asarum species. J Ethnopharmacol 2004;94:245-9
- Jiang X, Wang ZM, You LS, et al. [Determination of aristolochic acid A in Radix Aristolochiae and Herba Asari by RP-HPLC] (Chinese). Zhongguo Zhong Yao Za Zhi 2004;29:408-10
- Zhao ZZ, Liang ZT, Jiang ZH, et al. Comparative study on the aristolochic acid I content of Herba Asari for safe use. Phytomedicine 2008;15:741-8
- BfArM. Aristolochiaceaehaltige Arzneimittel, die unter Verwendung von Pflanzen der Gattung Asarum hergestellt werden: Das BfArM ordnet den Widerruf der Zulassung an. Bescheid vom 22.07.2010: http://www.bfarm.de/cae/servlet/contentblob/1207042/publicationFile/92601/aristolochia_bescheid.pdf, date accessed 2010 Sep 1, 2010
- N.N. Hormone nach den Wechseljahren: der Skandal setzt sich fort. arzneitelegramm 2002;33:81-3
- N. N. Blasenkrebs unter Pioglitazon (Actos u.a.). arzneitelegramm 2010;41:108
- Kvaavik E, Batty GD, Ursin G, et al. Influence of inpidual and combined health behaviors on total and cause-specific mortality in men and women: the United Kingdom health and lifestyle survey. Arch Intern Med 2010;170:711-8
- Bundesministerium der Justiz. Verordnung über den Schutz vor Schäden durch ionisierende Strahlen, 2008
- Schmitz-Feuerhake I. Übersicht zu den Langzeitfolgen von chronischer Niedrigdosisbestrahlung. Strahlentelex 2006;20(460-461):1-5
|
Spezies (Probe) |
Pflanzenteil |
Extraktion |
Herkunft |
AAI [μg/g] |
AAII [μg/g] |
Studie |
|
Asarum sieboldii |
radix(?) |
ME |
Japan |
< 1 |
< 1 |
Hashimoto 1999 |
|
Asarum sieboldii |
radix(?) |
ME |
Japan |
< 1 |
< 1 |
|
|
Asarum heterotropoides var. mandshuricum |
radix(?) |
ME |
China, Liaoning |
< 1 |
< 1 |
|
|
Asarum heterotropoides var. mandshuricum |
radix(?) |
ME |
China, Jilin |
< 1 |
< 1 |
|
|
Asarum heterotropoides var. mandshuricum |
radix(?) |
ME |
North Korea |
< 1 |
< 1 |
|
|
Asarum heterotropoides var. mandshuricum |
radix(?) |
ME |
Liaoning |
< 1 |
< 1 |
|
|
Asarum sieboldii var. seoulense |
radix(?) |
ME |
Korea |
< 1 |
< 1 |
|
|
Asarum heterotropoides var. mandshuricum |
herba(?) |
MEc |
China |
42.2 |
neg. |
Jong 2003 |
|
Asarum crispulatum (=alternate species) |
herba(?) |
MEc |
China |
3376.9 |
neg. |
|
|
Asarum sieboldii |
herba(?) |
MEc |
China |
3.3 |
neg. |
|
|
Asarum fukienense (=adulterant) |
herba(?) |
MEc |
China |
16.6 |
neg. |
|
|
Asarum fukienense (=adulterant) |
herba(?) |
MEh |
China |
11.7 |
neg. |
|
|
Asarum sieboldii |
herba(?) |
ME |
China |
neg. |
neg. |
Schaneberg 2004 |
|
Asarum heterotropoides var. mandshuricum |
herba |
ME |
Jilin |
50.69 |
Jiang 2004 |
|
|
Asarum sieboldii |
herba |
ME |
Jilin |
71.06 |
||
|
Asarum heterotropoides var. mandshuricum |
herba |
ME |
Jilin |
351.1 |
||
|
Asarum heterotropoides var. mandshuricum |
herba |
ME |
Liaoning |
26.47 |
||
|
Asarum sieboldii |
herba |
ME |
Liaoning |
145.0 |
||
|
Asarum heterotropoides var. mandshuricum |
herba |
ME |
Liaoning |
neg. |
||
|
Asarum sieboldii var. seoulense (A) |
radix |
ME |
Hong Kong |
0.19 |
Zhao 2008 |
|
|
Asarum sieboldii var. seoulense (A) |
radix |
WE |
Hong Kong |
0.04 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
herba |
ME |
Hong Kong |
11.91 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
herba |
WE |
Hong Kong |
0.34 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
planta tota |
ME |
Hong Kong |
5.30 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
planta tota |
WE |
Hong Kong |
0.25 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
radix |
ME |
Hong Kong |
2.16 |
||
|
Asarum heterotropoides var. mandshuricum (B) |
radix |
WE |
Hong Kong |
0.15 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
herba |
ME |
Hong Kong |
6.14 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
herba |
WE |
Hong Kong |
0.31 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
planta tota |
ME |
Hong Kong |
2.21 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
radix |
ME |
Hong Kong |
0.93 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
radix |
WE |
Hong Kong |
0.05 |
||
|
Asarum heterotropoides var. mandshuricum (C) |
planta tota |
WE |
Hong Kong |
0.09 |
Tab. 1: Gehalt an Aristolochiasäure-I (AA-I) bzw. Aristolochiasäure-II (AA-II) in verschiedenen Asarum-Spezies, unterschiedlichen Pflanzenteilen und unterschiedlichen Extrakten. Offizinelle Spezies mit dem Pflanzenteil Radix sind grün hinterlegt, mit anderen Pflanzenteilen gelb, nicht offizinelle Spezies sind braun hinterlegt. Gehalte von wässrigen Extrakten der offizinellen Drogen sind fett gedruckt, sie entsprechen in etwa einem Gehalt, der in einem Dekokt zu erwarten ist. ME = methanolische Extraktion, MEc = extrahiert mit kalten Methanol, MEh = extrahiert mit heißem Methanol, WE = wässrige Extraktion